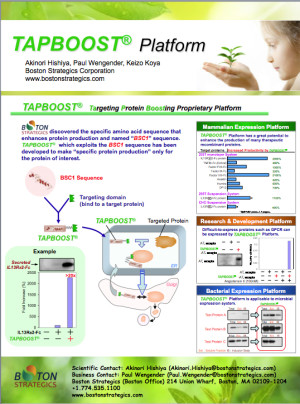
発表内容:E6201 — 難治性急性骨髄性白血病(AML)治療薬候補、チロシンキナーゼ阻害剤
ストラテジア製薬は、ボストンストラテジックス社として、2012年4月にマサチューセッツ州ボストンに本社を設立し、2013年11月にはテキサス州ヒューストン、テキサス医療センター近辺にヒューストン医薬研究開発センターを設立しました。2015年、ストラテジア製薬と改名し、ビジョンをさらに明確にすることで、既存の製薬パラダイムから抜け出し、独自のアプローチで医薬研究開発に取り組んでいます。新しい治療法を必要とする患者さんへ、より早く、より効果的に、より安く新薬をお届けすることを目指しています。
ストラテジア製薬は、国際的エキスパートの少数精鋭新薬開発プロジェクトチームを結成し、製薬会社とバイオテック企業の新薬開発研究を支援します。また、ストラテジア製薬の中核チームメンバーは、ディスカバリーからグローバルマーケットでの認可取得、および、ライフサイクル・マネージメントに及ぶ様々な領域で医薬開発専門知識を有し、その知識と経験、そして、ストラテジア製薬が築き上げたネットワークを最大限に駆使して、新薬研究開発に取り組んでいます
ストラテジア製薬は、日系製薬会社とパートナーシップを築き、米国での新薬開発戦略支援を中心に取り組んできました。アライアンス契約を結んだMDアンダーソンがんセンターをはじめとするテキサス州の医療機関との強い繋がりを構築し、プロジェクトチームのパートナーと共に、常に前臨床および臨床試験研究を積極的に行っています。
また、製薬会社と独占ライセンス契約を結び、その臨床段階の薬剤候補の医薬研究開発も行っています。ストラテジア製薬が研究開発している新薬候補であるE6201は、エーザイ株式会社により転移性メラノーマの治療薬として開発されていた薬剤で、ストラテジア社はエーザイ株式会社と独占ライセンス契約を結び、固形癌および血液癌治療のためのキナーゼ選択的二重阻害剤として研究開発をしています。E6201は、低分子のFms様チロシンキナーゼ3受容体 (FLT3)/マイトジェン活性化プロテインキナーゼ(MEK)の二重阻害剤で、再発性急性骨髄性白血病および難治性急性骨髄性白血病(AML)の患者さんの治療を目指して、臨床開発を進めています。また、次の薬剤候補のインライセンスを進めています。遺伝子突然変異の患者さん、また、一般的に使われている治療薬が効かない固形癌と血液癌の患者さんたちにとり、これらの薬剤は必要であると信じています。現在、これらの新薬研究開発を支援するために必要な資金を集めています
豊富な知識と経験を持つストラテジア製薬(ボストンとテキサス)のマネージメントチームは、前臨床、製剤製造、臨床開発、FDA申請書提出、メインテナンス、認可、および、ライフサイクル・マネージメントまでの実績を積んでいます。
連絡先:ストラテジア製薬 +1-781-761-0123 (ボストンオフィス電話番号)
Contact@StrategiaTx.com (連絡先Eメール)
StrategiaTx.com (ウェブサイト)